 (ほそや・ひろし)
(ほそや・ひろし)◇一九五六年 東京都生まれ
◇東京大学大学院理学系研究科生物化学専攻(博士)修了、理学博士
◇東京都臨床医学総合研究所勤務を経て一九九二年から本学勤務
◇理学部生物科学科教授
専門は分子細胞生物学
現在、「動物細胞の分裂メカニズムの解明」を主要テーマに、高等動物のガン細胞や原生動物を実験材料に研究を行っている。
hhosoya@sci.hiroshima-u.ac.jp
細胞が「分裂する」時に起こっていること |
プロフィール
 (ほそや・ひろし)
(ほそや・ひろし)◇一九五六年 東京都生まれ ◇東京大学大学院理学系研究科生物化学専攻(博士)修了、理学博士 ◇東京都臨床医学総合研究所勤務を経て一九九二年から本学勤務 ◇理学部生物科学科教授 専門は分子細胞生物学 現在、「動物細胞の分裂メカニズムの解明」を主要テーマに、高等動物のガン細胞や原生動物を実験材料に研究を行っている。 hhosoya@sci.hiroshima-u.ac.jp |
|
「一つの細胞が二つに分裂すること」を,細胞分裂(Cell Division)と呼ぶ。二つに分裂した細胞はその後どんどん増殖し,多細胞の新しい生命体が構築されていく。本稿では,生命の基本現象である「細胞分裂」のメカニズム解明に関する最新の知見を紹介する。
|
|
研究の背景 |
|
実験材料について |
|
細胞のくびれと収縮環 |
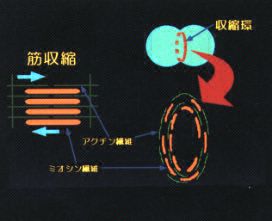 図1:収縮環と筋肉の模式図 |
|
収縮環の収縮メカニズムは? |
|
〈平滑筋の収縮〉 (1)細胞内Ca2+濃度の上昇 ↓ (2)Ca2+/カルモジュリンによるミオシン軽鎖キナーゼ(MLCK)の活性化 ↓ (3)ミオシン軽鎖のリン酸化 ↓ (4)ミオシンの活性化(ATPアーゼ活性の上昇) ↓ (5)アクチン繊維とミオシン繊維のすべり ↓ (6)平滑筋の収縮 |
| 図2:平滑筋収縮のメカニズム (「広島大学低温センターだより」1997年9月号より引用) |
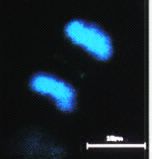 図3:分裂細胞の「くびれ=収縮環」に局在するリン酸化ミオシン(緑色の蛍光染色部)。青い部分は,染色体DNA。バーの長さは10ミクロン |
|
リン酸化されたミオシンが収縮環に局在する |
|
ミオシン(軽鎖)をリン酸化するキナーゼ |
|
ミドリゾウリムシを「細胞分裂」の研究に使うこと |
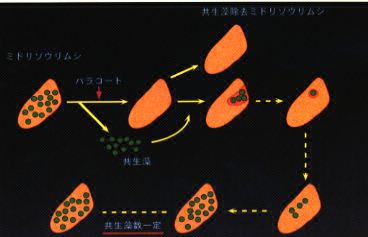 図4:「ミドリゾウリムシ共生藻のクローン化と再共生」の概念図。 パラコート(農薬。光合成の阻害剤)をミドリゾウリムシに作用させると,植物である共生藻が姿を消してしまい,動物であるミドリゾウリムシは元気である。共生藻を食べさせると(図中の赤い部分がミドリゾウリムシの食胞),大部分が消化されるが,一部が生き残ってミドリゾウリムシ体内で増殖を開始する(=再共生)。 なぜ,これらの共生藻は,生き残れるのだろうか。(西原直久(D3,学振DC2特別研究員)原図より) |
|
あとがき |